Ikatan Kimia: Perbedaan dan Rumus Ikatan Kovalen, Ionik, dan Logam
Ikatan kimia adalah gaya tarik-menarik yang menghubungkan atom-atom dalam suatu senyawa atau molekul. Proses pembentukan ikatan kimia memungkinkan atom-atom untuk mencapai login neymar8 konfigurasi elektron yang lebih stabil. Ada tiga jenis ikatan kimia utama yang umum ditemukan dalam berbagai senyawa, yaitu ikatan kovalen, ionik, dan logam. Masing-masing memiliki karakteristik yang membedakan satu dengan yang lainnya, baik dalam hal sifat fisik, struktur, maupun cara terbentuknya.
Baca juga:
Rumus Dasar Matematika yang Wajib Diketahui Siswa SD hingga SMA
1. Ikatan Kovalen
Ikatan kovalen terbentuk ketika dua atom saling berbagi pasangan elektron. Ikatan ini terjadi antara dua non-logam yang memiliki kecenderungan untuk berbagi elektron agar mencapai kestabilan elektron. Pada ikatan kovalen, tidak ada pemindahan elektron, hanya berbagi.
-
Ciri-ciri Ikatan Kovalen:
-
Atom-atom yang terlibat adalah non-logam (seperti hidrogen, oksigen, karbon).
-
Elektron dibagikan secara merata atau tidak merata antara dua atom.
-
Ikatan ini memiliki titik leleh dan didihkan yang relatif rendah.
-
Ikatan kovalen menghasilkan molekul yang netral (tidak bermuatan).
-
Contoh senyawa kovalen: H₂O (air), CO₂ (karbon dioksida), O₂ (oksigen).
-
-
Contoh Rumus Ikatan Kovalen:
-
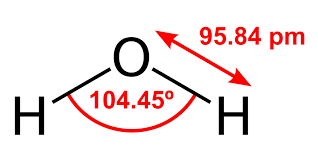
H₂O (Air): Atom hidrogen (H) berbagi satu elektron dengan atom oksigen (O) untuk membentuk dua ikatan kovalen tunggal. H₂O memiliki struktur molekul berbentuk sudut.
-
2. Ikatan Ionik
Ikatan ionik terbentuk ketika satu atom menyerahkan elektron kepada atom lainnya, sehingga membentuk ion dengan muatan berlawanan yang saling tarik menarik. Ikatan ini biasanya terjadi antara atom logam dan non-logam. Atom logam cenderung melepaskan elektron, sementara atom non-logam cenderung menerima elektron untuk membentuk ion negatif.
-
Ciri-ciri Ikatan Ionik:
-
Terjadi antara logam dan non-logam.
-
Satu atom melepaskan elektron (membentuk ion positif atau kation), sedangkan atom lainnya menerima elektron (membentuk ion negatif atau anion).
-
Senyawa ionik umumnya memiliki titik leleh dan titik didih yang tinggi.
-
Ikatan ionik terbentuk dalam kristal yang memiliki struktur yang teratur.
-
Senyawa ionik sering larut dalam air dan dapat menghantarkan listrik ketika terlarut.
-
Contoh senyawa ionik: NaCl (garam dapur), MgO (magnesium oksida).
-
-
Contoh Rumus Ikatan Ionik:
-
NaCl (Natrium klorida): Atom natrium (Na) melepaskan satu elektron untuk membentuk ion Na⁺, sedangkan atom klor (Cl) menerima elektron tersebut untuk membentuk ion Cl⁻. Ikatan antara kedua ion yang bermuatan ini membentuk kristal garam.
-
3. Ikatan Logam
Ikatan logam terjadi ketika atom-atom logam berbagi elektron secara bebas dalam struktur yang dikenal sebagai “lautan elektron.” Pada ikatan logam, elektron-elektron valensi bergerak bebas di antara ion-ion logam yang teratur, sehingga menciptakan ikatan yang kuat antar atom logam.
-
Ciri-ciri Ikatan Logam:
-
Terjadi antar atom logam (seperti tembaga, besi, dan aluminium).
-
Elektron-elektron valensi bergerak bebas dalam struktur logam.
-
Memiliki daya hantar listrik yang sangat baik karena adanya pergerakan elektron bebas.
-
Memiliki titik leleh dan titik didih yang tinggi.
-
Biasanya bersifat ulet dan dapat dibentuk menjadi berbagai bentuk (misalnya kawat).
-
Contoh senyawa logam: Fe (besi), Cu (tembaga), Al (aluminium).
-
-
Contoh Rumus Ikatan Logam:
-
Cu (Tembaga): Pada tembaga, atom-atomnya berbagi elektron-elektron valensi yang dapat bergerak bebas di antara ion-ion tembaga, menciptakan ikatan logam yang kuat dan memungkinkan tembaga untuk menghantarkan listrik.
-
Perbedaan Antara Ikatan Kovalen, Ionik, dan Logam
| Karakteristik | Ikatan Kovalen | Ikatan Ionik | Ikatan Logam |
|---|---|---|---|
| Jenis Atom | Non-logam + Non-logam | Logam + Non-logam | Logam + Logam |
| Pembentukan Elektron | Berbagi elektron | Pemindahan elektron | Elektron bergerak bebas |
| Sifat Fisik | Titik leleh rendah, molekul | Titik leleh tinggi, padat, keras | Daya hantar listrik baik, ulet |
| Contoh Senyawa | H₂O, CO₂, NH₃ | NaCl, MgO, KCl | Fe, Cu, Al |
Kesimpulan
Ikatan kovalen, ionik, dan logam memiliki karakteristik yang sangat berbeda meskipun semuanya memainkan peran penting dalam pembentukan senyawa kimia. Pemahaman mengenai jenis-jenis ikatan ini membantu kita dalam mempelajari berbagai sifat fisik dan kimia senyawa, serta aplikasinya dalam kehidupan sehari-hari, seperti dalam pembuatan material, penghantar listrik, dan banyak lagi
Leave a Reply